ผู้เขียน:
Mike Robinson
วันที่สร้าง:
7 กันยายน 2021
วันที่อัปเดต:
11 พฤษภาคม 2024

เนื้อหา
เลขอะตอมสอดคล้องกับจำนวนโปรตอนในนิวเคลียสของอะตอมเดียวของธาตุ ค่านี้ไม่เปลี่ยนแปลง ดังนั้นคุณสามารถใช้เพื่อค้นหาลักษณะอื่น ๆ ของไอโซโทปเช่นจำนวนนิวตรอน
ขั้นตอน
ส่วนที่ 1 ของ 2: การหาเลขอะตอม
ค้นหาสำเนาตารางธาตุ คลิกที่นี่หากคุณไม่มี แต่ละองค์ประกอบมีเลขอะตอมของตัวเอง ดังนั้นจึงไม่มีทางลัดในการเรียนรู้เนื้อหา ใช้สำเนาตารางหรือพยายามจดจำ
- หนังสือเคมีส่วนใหญ่จะมีตารางพิมพ์อยู่ที่ปกหลัง

ค้นหาองค์ประกอบที่คุณกำลังศึกษาอยู่ในตาราง ตารางส่วนใหญ่จะมีชื่อเต็มขององค์ประกอบตลอดจนสัญลักษณ์ (เช่นปรอทเป็นต้น) หากคุณไม่พบสิ่งที่ต้องการค้นหาให้ออนไลน์และทำการค้นหาด้วยคำว่า "สัญลักษณ์ทางเคมี" และชื่อขององค์ประกอบ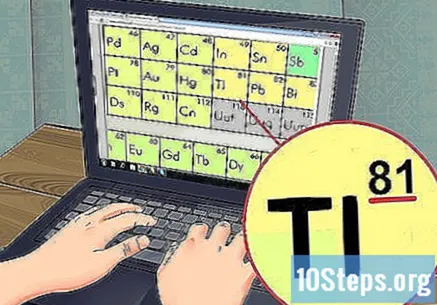
ค้นหาเลขอะตอมของธาตุ โดยปกติจะอยู่ที่มุมบนซ้ายหรือขวาของบ้านขององค์ประกอบ แต่ก็สามารถเข้ามาในที่อื่นได้เช่นกัน นอกจากนี้ยังเป็นค่าจำนวนเต็มเสมอ- หากตัวเลขมีจุดทศนิยมแสดงว่าอาจเป็นมวลอะตอม
ยืนยันข้อมูลตามองค์ประกอบใกล้เคียง ตารางธาตุจัดตามลำดับเลขอะตอม ตัวอย่างเช่นหากหมายเลขไอโซโทปของคุณคือ "33" องค์ประกอบทางด้านซ้ายจะเป็น "32" และองค์ประกอบทางด้านขวาจะเป็น "34" ในกรณีนี้เป็นเพราะคุณกำลังดูเลขอะตอม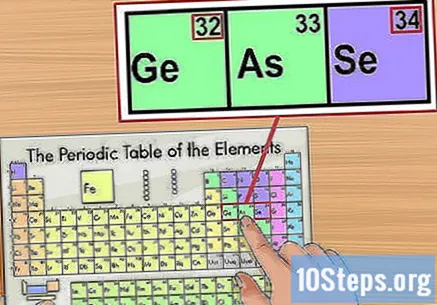
- มีการกระโดดระหว่างองค์ประกอบ "56" (แบเรียม) และ "88" (วิทยุ) ไอโซโทปที่สอดคล้องกับช่วงนี้อยู่ในสองแถวด้านล่างตาราง จะแยกเฉพาะแบบนี้เพื่อไม่ให้โต๊ะใหญ่เกินไป
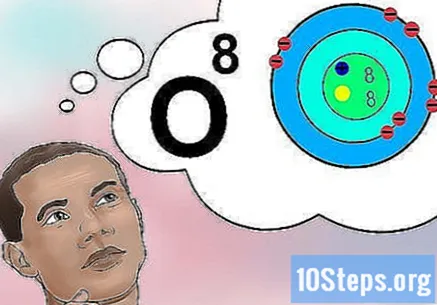
ทำความเข้าใจว่าเลขอะตอมหมายถึงอะไร เลขอะตอมมีคำจำกัดความง่ายๆคือปริมาณโปรตอนในอะตอมของธาตุ ในทางกลับกันจำนวนโปรตอนนี้จะเป็นตัวกำหนดประจุไฟฟ้าทั้งหมดของนิวเคลียสซึ่งจะกำหนดจำนวนอิเล็กตรอนที่อะตอมสามารถชาร์จได้ เนื่องจากอิเล็กตรอนมีหน้าที่ในการโต้ตอบทางเคมีเกือบทั้งหมดเลขอะตอมจึงส่งผลทางอ้อมต่อคุณสมบัติทางกายภาพและทางเคมีของธาตุ- กล่าวอีกนัยหนึ่งอะตอมที่มีโปรตอนแปดตัวจะสอดคล้องกับอะตอมของออกซิเจน อะตอมของออกซิเจนสองตัวสามารถมีจำนวนนิวตรอนต่างกันหรือ (ถ้าเป็นไอออน) หรืออิเล็กตรอน แต่จะมีโปรตอนแปดตัวเสมอ
ส่วนที่ 2 ของ 2: การค้นพบข้อมูลที่สำคัญมากขึ้น
กำหนดน้ำหนักอะตอม โดยปกติจะอยู่ภายใต้ชื่อขององค์ประกอบในตารางธาตุและมีทศนิยมสองหรือสามตำแหน่ง น้ำหนักอะตอมสอดคล้องกับมวลเฉลี่ยของอะตอมของธาตุซึ่งแสดงถึงลักษณะที่พบในธรรมชาติ มีหน่วยวัดเป็น "หน่วยมวลอะตอม" ("u" หรือ "u.m.a")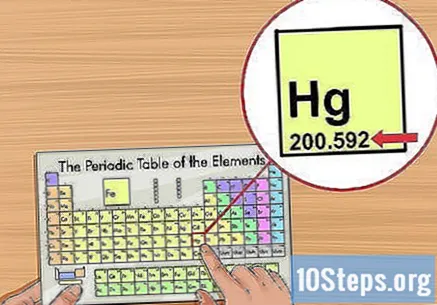
- นักวิทยาศาสตร์หลายคนชอบใช้คำว่ามวลอะตอมแทนน้ำหนัก
ทำความเข้าใจเกี่ยวกับมวลอะตอม แนวคิดเรื่องมวลอะตอมนั้นคล้ายคลึงกับน้ำหนักมาก ความแตกต่างคือน้ำหนักบ่งบอกมวลเฉลี่ยของอะตอมใด ๆ ในองค์ประกอบไม่ใช่อะตอมเฉพาะ ตัวอย่างเช่นเหล็ก 1 กรัมประกอบด้วยอะตอมหลายอะตอมที่มีมวลต่างกัน น้ำหนักบ่งบอกถึง "มวลสัมพัทธ์" หากคุณศึกษาอะตอมเดี่ยวของธาตุคุณเพียงแค่ต้องรู้มวลเฉพาะของมัน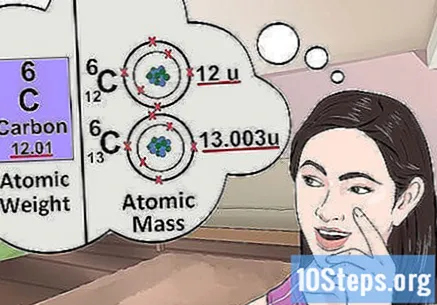
- โดยทั่วไปปัญหาทางเคมีที่เกี่ยวข้องกับอะตอมเพียงอย่างเดียวจะแจ้งเลขมวลอะตอมอยู่แล้ว คุณเพียงแค่ต้องเข้าใจแนวคิดเพื่อไม่ให้ระวังเมื่อคุณเห็นคุณค่าที่แตกต่างออกไป
ปัดเศษเลขมวล เลขมวลสอดคล้องกับจำนวนโปรตอนและนิวตรอนทั้งหมดในอะตอมของธาตุ คำนวณได้ไม่ยากเพียงแค่นำมวลอะตอมที่พิมพ์บนตารางธาตุแล้วปัดเศษให้เป็นค่าทั้งหมดที่ใกล้เคียงที่สุด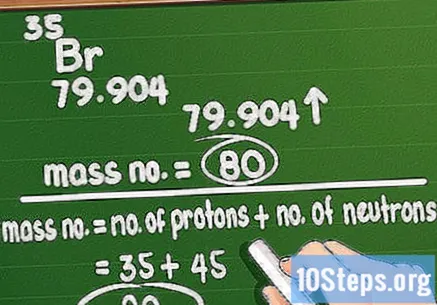
- สิ่งนี้ได้ผลเนื่องจากจำนวนนิวตรอนและโปรตอนอยู่ใกล้ 1 u.m.a ในขณะที่อิเล็กตรอนมีค่าใกล้ศูนย์มาก มวลอะตอมเกี่ยวข้องกับการคำนวณที่แน่นอนเพื่อหาค่าทศนิยม แต่ข้อมูลเดียวที่สำคัญคือตัวเลขทั้งหมดซึ่งบอกคุณว่ามีโปรตอนและนิวตรอนจำนวนเท่าใด
- จำไว้ว่าถ้าคุณใช้มวลอะตอมคุณจะยุ่งกับน้ำหนักของอะตอมเฉพาะในองค์ประกอบ ตัวอย่างเช่นโบรมีนมีมวลอะตอม 79 หรือ 81
คำนวณจำนวนนิวตรอน ตอนนี้คุณรู้แล้วว่าเลขอะตอมเท่ากับจำนวนโปรตอนและเลขมวลเท่ากับผลรวมของจำนวนโปรตอนและนิวตรอน ในการกำหนดจำนวนนิวตรอนในองค์ประกอบเพียงแค่ลบเลขอะตอมออกจากมวลทั้งหมดนั้น ตัวอย่างบางส่วน:
- อะตอมของฮีเลียม (He) มีเลขมวล 4 และเลขอะตอม 2 ดังนั้น 4 - 2 = 2 นิวตรอน.
- ตัวอย่างเงิน (Ag) มีเลขมวลเฉลี่ย 108 (ตามตารางธาตุ) และเลขอะตอม 47 โดยเฉลี่ยแล้วแต่ละอะตอมในตัวอย่างมี 108 - 47 = 61 นิวตรอน.
ทำความเข้าใจไอโซโทป ไอโซโทปเป็นรูปแบบเฉพาะขององค์ประกอบซึ่งประกอบด้วยนิวตรอนจำนวนหนึ่ง หากปัญหาที่คุณต้องการแก้ทำให้เกิดบางอย่างเช่น "โบรอน -10" หรือ "B" นั่นเป็นเพราะคุณกำลังพูดถึงองค์ประกอบของโบรอนที่มีเลขมวล 10 ให้ใช้ค่านี้ไม่ใช่ค่า "ปกติ" ของโบรอน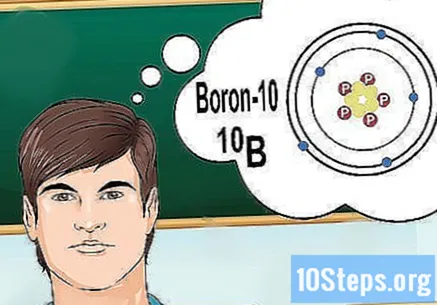
- เลขอะตอมของไอโซโทปไม่เคยเปลี่ยนแปลง ทุกไอโซโทปของธาตุมีจำนวนโปรตอนเท่ากัน
เคล็ดลับ
- น้ำหนักอะตอมของธาตุที่หนักกว่าบางส่วนอยู่ในวงเล็บหรือวงเล็บเหลี่ยม ซึ่งหมายความว่าน้ำหนักนี้เป็นมวลที่แน่นอนของไอโซโทปที่เสถียรที่สุดไม่ใช่ค่าเฉลี่ยของไอโซโทปหลายตัว สุดท้ายนี้ไม่มีผลต่อเลขอะตอมของธาตุ


