![🧪พันธะโคเวเลนต์ 8 : สภาพขั้วของโมเลกุลโคเวเลนต์ [Chemistry#56]](https://i.ytimg.com/vi/jQGkyZis9Os/hqdefault.jpg)
เนื้อหา
โมเลกุลคือชุดของอะตอมที่ยึดติดกัน ในบางกรณีการเชื่อมต่อดังกล่าวทำให้ประจุไฟฟ้ากระจายไปทั่วโมเลกุลไม่สม่ำเสมอทำให้เกิดขั้วสองขั้วขั้วบวกหนึ่งขั้วและขั้วลบหนึ่งขั้ว เมื่อสิ่งนี้เกิดขึ้นโมเลกุลจะเรียกว่าขั้ว คุณสามารถตรวจสอบได้ว่าโมเลกุลมีขั้วหรือไม่มีขั้วโดยการวิเคราะห์พันธะระหว่างอะตอมทดสอบปฏิกิริยาของมันเมื่อสัมผัสกับสารอื่น ๆ ที่มีขั้วหรือดูว่ามันทำงานอย่างไรเมื่อสัมผัสกับสนามแม่เหล็กไฟฟ้า
ขั้นตอน
วิธีที่ 1 จาก 3: การออกแบบโครงสร้าง Lewis Point
เขียนสัญลักษณ์ของอะตอมในโมเลกุล หากต้องการค้นหาสัญลักษณ์ของแต่ละอะตอมโปรดดูตารางธาตุ สัญลักษณ์ทางเคมีใช้แทนอะตอมในโครงสร้างลิวอิสดอท ระวังอย่าให้สับสน
- ในการสร้างโครงสร้างของโมเลกุลของน้ำเช่นสร้าง O และ H สองตัว
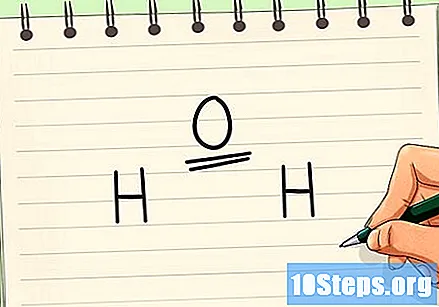
ค้นหาว่าอะตอมใดเป็นอะตอมกลาง อะตอมกลางคือสิ่งที่เชื่อมต่อกับอื่น ๆ ทั้งหมด (หรือเกือบทั้งหมด) นอกจากนี้ยังเป็นไปได้ที่อะตอมอื่น ๆ จะผูกมัดซึ่งกันและกัน โดยปกติอะตอมกลางจะมีค่าอิเล็กโทรเนกาติวิตีต่ำ- ข้อยกเว้นของกฎคือโมเลกุลของน้ำซึ่งมีอะตอมของออกซิเจนเป็นศูนย์กลางแม้ว่าจะมีอิเล็กโทรเนกาติวิตีมากกว่าอะตอมของไฮโดรเจนก็ตาม
- คาร์บอนไดออกไซด์เป็นตัวอย่างของโมเลกุลที่มีอะตอมอิเล็กโทรเนกาติวิตีน้อยที่สุดเป็นศูนย์กลาง
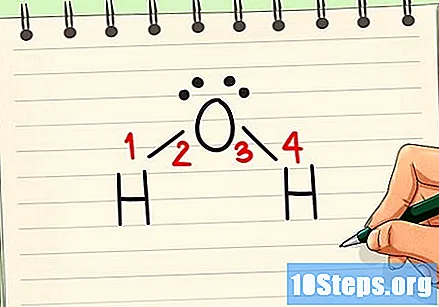
วาดพันธะเคมี ใช้กฎออกเตตเพื่อหาจำนวนพันธะในโมเลกุลและประเภทของพันธะ แต่ละอะตอมจะต้องมีอิเล็กตรอนแปดตัวในเปลือกวาเลนซ์เพื่อให้คงตัว บางคนต้องโทรสองหรือสามครั้งเพื่อให้ได้ความเสถียร- ทำการเชื่อมต่อระหว่างออกซิเจนกับอะตอมของไฮโดรเจนแต่ละอะตอม อะตอมของไฮโดรเจนไม่สร้างพันธะซึ่งกันและกัน

รวมอิเล็กตรอนที่ไม่มีพันธะในโครงสร้าง แม้ว่าอิเล็กตรอนส่วนใหญ่จะใช้ร่วมกันในพันธะเคมี แต่อะตอมบางชนิดก็มีอิเล็กตรอนที่ไม่ผูกมัด อิเล็กตรอนเหล่านี้จะต้องรวมอยู่ในโครงสร้างลิวอิสด้วยเนื่องจากมีความสำคัญอย่างยิ่งในการกำหนดขั้วของโมเลกุล สร้างจุดรอบ ๆ อะตอมเพื่อแทนอิเล็กตรอนลิแกนด์หรือไม่ของแต่ละตัว- ออกซิเจนมีอิเล็กตรอนที่ไม่มีพันธะสองคู่นั่นคือซึ่งติดอยู่กับอะตอมโดยไม่มีการใช้ร่วมกันในการเชื่อมต่อใด ๆ
ดูว่าโมเลกุลมีไดโพลหรือไม่. ไดโพลเกิดขึ้นเมื่อมีการกระจายอิเล็กตรอนในลักษณะของโมเลกุล การมีไดโพลหมายความว่าโมเลกุลมีขั้ว ถ้าอิเล็กตรอนมีการกระจายอย่างเท่าเทียมกันโมเลกุลจะไม่มีขั้ว
- เนื่องจากอิเล็กตรอนถูกดึงดูดให้ออกซิเจนมากกว่าไฮโดรเจนจึงมีแนวโน้มที่จะกระจุกตัวอยู่ที่ด้านนั้นของโมเลกุล สิ่งนี้ทำให้ออกซิเจนมีประจุลบและไฮโดรเจนมีประจุบวกสร้างไดโพลและทำให้น้ำเป็นโมเลกุลที่มีขั้ว
วิธีที่ 2 จาก 3: การทดสอบสารในตัวทำละลาย
เติมน้ำบีกเกอร์. น้ำเป็นตัวทำละลายที่มีขั้ว: ใส่ 100 มล. ลงในบีกเกอร์ที่สะอาดแล้วพักไว้
เติมบีกเกอร์อื่นด้วยตัวทำละลายที่ไม่มีขั้ว ตัวอย่างบางส่วนของตัวทำละลายที่ไม่มีขั้ว ได้แก่ โทลูอีนน้ำมันเบนซินและน้ำมันโดยทั่วไป ใส่ตัวทำละลายที่ไม่มีขั้ว 100 มล. ลงในบีกเกอร์อื่นแล้วพักไว้พร้อมกับน้ำ
- ตัวทำละลายที่ไม่มีขั้วหลายชนิดเป็นสารประกอบอินทรีย์ระเหยง่าย (VOCs) และอาจเป็นอันตรายได้ ระมัดระวังเมื่อให้ความร้อนและสวมถุงมือและหน้ากากเพื่อป้องกันตัวเอง
- น้ำมันพืชเป็นตัวทำละลายที่ไม่ระเหยง่ายซึ่งสามารถใช้ในบีกเกอร์ที่สองได้
- อะซิโตนเป็นตัวทำละลายอินทรีย์ที่ค่อนข้างปลอดภัย อย่างไรก็ตามเนื่องจากเป็นสารประกอบที่ระเหยได้จึงต้องเก็บให้ห่างจากไฟและใช้ถุงมือและหน้ากากป้องกัน
ใส่สารในปริมาณเท่า ๆ กันลงในบีกเกอร์ทั้งสอง ใส่สารที่เลือกไว้ในภาชนะทั้งสองโดยระมัดระวังในการใช้ในปริมาณที่เท่ากัน เริ่มต้นด้วยการเติมสาร 10 ถึง 20 กรัมลงในบีกเกอร์แต่ละอันหรือ 10 ถึง 20 มล. หากเป็นของเหลว
- คุณสามารถใส่ไอโซโพรพิลแอลกอฮอล์ 20 มล. ลงในบีกเกอร์แต่ละอันได้เช่น
ผัดส่วนผสมให้ร้อน คุณอาจต้องให้ความร้อนหรือกวนตัวทำละลายเพื่อให้สารมีปฏิกิริยาต่อกัน ตัวทำละลายทั้งสองต้องผสมและให้ความร้อนเท่า ๆ กัน โปรดจำไว้ว่าการให้ความร้อนกับตัวทำละลายอินทรีย์เช่นโทลูอีนอาจเป็นอันตรายได้ ดูแลพวกเขาเป็นอย่างดี
- หากคุณใช้ไอโซโพรพิลแอลกอฮอล์เพียงแค่กวนสารละลายเพื่อเปิดใช้งาน ไม่จำเป็นต้องร้อนขึ้น
- ใช้แผ่นร้อนค่อยๆให้ส่วนผสมร้อนขึ้น อย่าใส่ตัวทำละลายอินทรีย์ลงในกองไฟ
ปล่อยให้บีกเกอร์เย็นลง หลังจากที่สารเริ่มทำปฏิกิริยากับตัวทำละลายหนึ่งตัวหรือทั้งสองตัวให้ปล่อยให้สารผสมเย็นตัวลง สิ่งนี้จะทำให้สารแยกตัวออกจากตัวทำละลายหากเข้ากันไม่ได้นอกจากจะอำนวยความสะดวกในการทำงานแล้ว
สังเกตผลลัพธ์. ดูว่ามีสารที่เป็นของแข็งหรือของเหลวแยกออกจากตัวทำละลายหรือไม่ ถ้าเป็นเช่นนั้นแสดงว่าสารนั้นเข้ากันไม่ได้กับตัวทำละลายนั้น โมเลกุลมีขั้วเข้ากันได้กับตัวทำละลายที่มีขั้วและโมเลกุลที่ไม่มีขั้วกับตัวทำละลายที่ไม่มีขั้ว ดังนั้นสารใด ๆ ที่ละลายในน้ำจึงมีขั้ว สารที่ไม่ละลายในน้ำ แต่เข้ากันได้กับน้ำมันเบนซินโทลูอีนอะซิโตนหรือตัวทำละลายที่ไม่มีขั้วอื่น ๆ ก็ไม่มีขั้วเช่นกัน
- เมื่อส่วนผสมทั้งสองพร้อมกันไอโซโพรพิลแอลกอฮอล์จะละลายในน้ำจนหมด แต่จะสร้างน้ำมันพืชแยกชั้นในบีกเกอร์ที่สอง นั่นหมายความว่าไอโซโพรพิลแอลกอฮอล์มีขั้ว
วิธีที่ 3 จาก 3: ทดสอบโมเลกุลด้วยแม่เหล็กไฟฟ้า
วางสารใกล้แม่เหล็ก คุณสามารถตรวจสอบได้ว่าสารมีขั้วหรือไม่มีขั้วโดยการเข้าหาแม่เหล็กหรือวัตถุที่มีประจุแม่เหล็กขนาดใหญ่ รองรับสารบนม้านั่งและนำแม่เหล็กเข้ามาใกล้โดยไม่ต้องสัมผัส
ดูว่ามีปฏิกิริยาใด ๆ ถ้าแม่เหล็กถูกดึงดูดหรือขับไล่ด้วยสารแสดงว่ามีขั้ว อย่างไรก็ตามการไม่มีปฏิกิริยาไม่ได้หมายความว่าสารนั้นไม่มีขั้ว โมเลกุลที่มีขั้วบางชนิดมีขั้วไม่เพียงพอที่จะทำให้เกิดปฏิกิริยาแม่เหล็กอย่างอ่อน
- ตัวอย่างเช่นหากคุณเคลื่อนแม่เหล็กเข้าใกล้กระแสน้ำที่ไหลจะทำให้ของเหลวเบี่ยงเบนซึ่งบ่งบอกถึงปฏิกิริยาที่ชัดเจนต่อสนามแม่เหล็กไฟฟ้า
นำสารเข้าไมโครเวฟ. เตาอบไมโครเวฟใช้รังสีแม่เหล็กไฟฟ้าความถี่สูงเพื่อปั่นโมเลกุลของอาหารสร้างแรงเสียดทานและความร้อน ในการทดสอบขั้วของสารให้วางในไมโครเวฟ
- ห้ามนำวัสดุที่เป็นโลหะไวไฟหรือระเบิดเข้าไมโครเวฟ
- เมื่อวางในไมโครเวฟน้ำจะร้อนซึ่งหมายความว่ามีขั้ว
- ในทางกลับกันน้ำมันแร่ไม่ได้รับความร้อนอย่างดีเมื่อนำเข้าไมโครเวฟซึ่งหมายความว่าไม่มีขั้ว
เปิดไมโครเวฟ. เมื่อสัมผัสกับรังสีแม่เหล็กไฟฟ้าโมเลกุลของสารจะเริ่มหมุน คุณจะไม่สามารถมองเห็นปรากฏการณ์นี้ได้ แต่หมายความว่าสารนั้นมีขั้ว หากเป็นแบบไม่มีขั้วจะไม่ได้รับการเปลี่ยนแปลงใด ๆ ในไมโครเวฟ
สังเกตสาร. ดูว่ามันร้อนและมีร่องรอยการหลอมละลายหรือผิดรูปหรือไม่ หากได้รับผลกระทบจากรังสีไมโครเวฟแสดงว่ามีขั้ว