เนื้อหา
แม้ว่าอะตอมทั้งหมดของธาตุเดียวกันจะมีจำนวนโปรตอนเท่ากัน แต่จำนวนนิวตรอนอาจแตกต่างกันไป การรู้ว่าอะตอมหนึ่ง ๆ มีจำนวนนิวตรอนเท่าใดสามารถช่วยให้คุณทราบได้ว่าอนุภาคนั้นเป็นอนุภาคปกติในองค์ประกอบนั้นหรือเป็นไอโซโทปซึ่งจะมีนิวตรอนมากหรือน้อย การหาจำนวนนิวตรอนในอะตอมนั้นค่อนข้างง่ายและไม่ต้องมีการทดลองใด ๆ ในการคำนวณจำนวนนิวตรอนในอะตอมหรือไอโซโทปปกติให้ทำตามคำแนะนำเหล่านี้พร้อมกับตารางธาตุในมือ
ขั้นตอน
วิธีที่ 1 จาก 2: การหาจำนวนนิวตรอนในอะตอมทั่วไป
ค้นหาองค์ประกอบในตารางธาตุ สำหรับตัวอย่างนี้เรามาดู OS (OS) ซึ่งอยู่ในแถวที่หกจากบนลงล่าง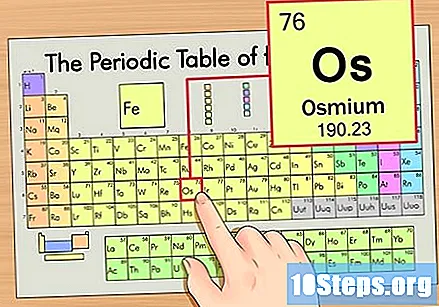
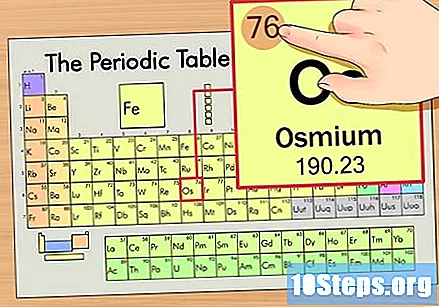
ค้นหาเลขอะตอมของธาตุ โดยปกติจะเป็นตัวเลขที่มองเห็นได้ชัดเจนที่สุดสำหรับองค์ประกอบหนึ่ง ๆ และโดยปกติจะอยู่เหนือสัญลักษณ์ของมัน (ในตารางที่เราใช้ในความเป็นจริงไม่มีตัวเลขอื่นอยู่ในรายการ) เลขอะตอมคือจำนวนโปรตอนในอะตอมเดียวของธาตุนั้น. จำนวนของ Os คือ 76 ซึ่งหมายความว่าอะตอมของ Osmium มีโปรตอน 76 ตัว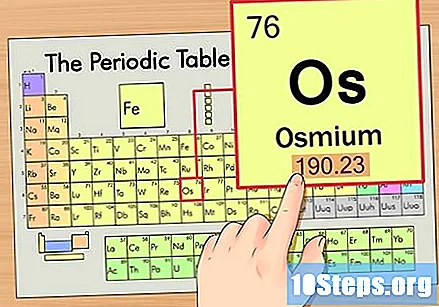
หาน้ำหนักอะตอมของธาตุ โดยปกติตัวเลขนี้จะอยู่ด้านล่างสัญลักษณ์อะตอม โปรดทราบว่าตารางในตัวอย่างนี้อ้างอิงจากเลขอะตอมเท่านั้นและไม่ได้แสดงรายการน้ำหนักอะตอม ซึ่งจะไม่เป็นเช่นนั้นเสมอไป ออสเมียมมีน้ำหนักอะตอม 190.23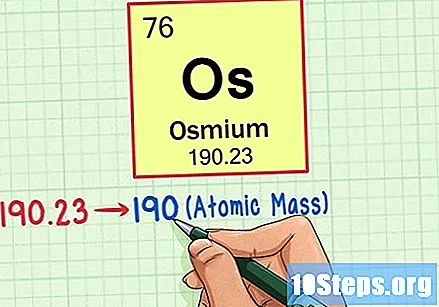
ปัดน้ำหนักอะตอมให้เป็นจำนวนเต็มที่ใกล้ที่สุดเพื่อหามวลอะตอม ในตัวอย่างของเรา 190.23 จะถูกปัดเศษเป็น 190 ทำให้มีมวลอะตอม 190 สำหรับออสเมียม- มวลอะตอมเป็นค่าเฉลี่ยของไอโซโทปของธาตุ ดังนั้นจึงมักไม่เป็นจำนวนเต็ม
ลบเลขอะตอมออกจากมวลอะตอม เนื่องจากมวลส่วนใหญ่ของอะตอมพบในโปรตอนและนิวตรอนการลบจำนวนโปรตอน (นั่นคือเลขอะตอม) ออกจากมวลอะตอมจะทำให้คุณได้จำนวน คำนวณ ของนิวตรอนในอะตอม โดยทั่วไปแล้วจำนวนหลังจุดทศนิยมจะแสดงถึงมวลของอิเล็กตรอนที่มีขนาดเล็กมากในอะตอม ในตัวอย่างของเรานี่คือ 190 (มวลอะตอม) - 76 (จำนวนโปรตอน) = 114 (จำนวนนิวตรอน)
จำสูตร. หากต้องการหาจำนวนนิวตรอนในอนาคตให้ใช้สูตรนี้: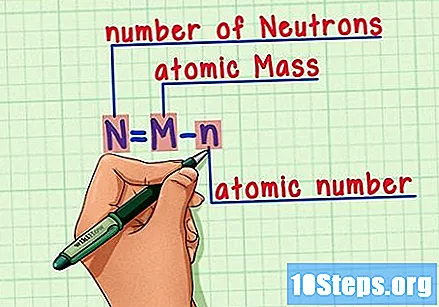
- N = M - น.
- N = จำนวน ยังไม่มีข้อความeutrons
- M = Mปรมาณูย่าง.
- n = nกระดูกต้นแขน
- N = M - น.
วิธีที่ 2 จาก 2: การหาจำนวนนิวตรอนในไอโซโทป
ค้นหาองค์ประกอบในตารางธาตุ ตัวอย่างเช่นลองใช้ไอโซโทปของคาร์บอน -14 เนื่องจากรูปแบบที่ไม่ใช่ไอโซโทปของคาร์บอน -14 เป็นเพียงคาร์บอน (C) ให้ค้นหาองค์ประกอบนี้ในตารางธาตุ (ในแถวที่สอง)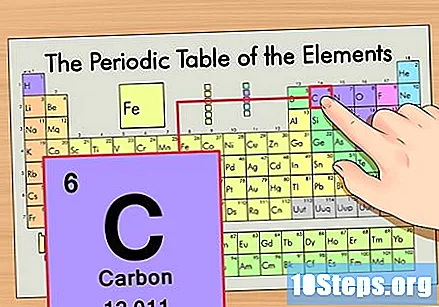
ค้นหาเลขอะตอมของธาตุ โดยปกติจะเป็นตัวเลขที่มองเห็นได้ชัดเจนที่สุดสำหรับองค์ประกอบหนึ่ง ๆ และโดยปกติจะอยู่เหนือสัญลักษณ์ของมัน (ในตารางที่เราใช้ในความเป็นจริงไม่มีตัวเลขอื่นอยู่ในรายการ) เลขอะตอมคือจำนวนโปรตอนในอะตอมเดียวของธาตุนั้น. C คือเลข 6 ซึ่งหมายความว่าอะตอมของคาร์บอนมี 6 โปรตอน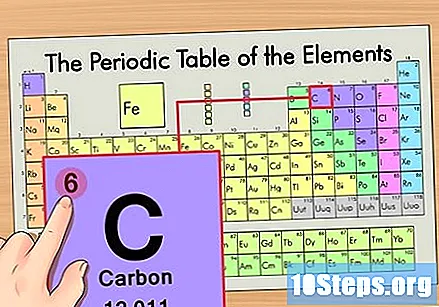
หามวลอะตอม. นี่เป็นเรื่องง่ายอย่างเหลือเชื่อสำหรับไอโซโทปเนื่องจากมีการตั้งชื่อตามมวลอะตอม คาร์บอน -14 มีมวลอะตอมเท่ากับ 14 เมื่อคุณพบมวลอะตอมของไอโซโทปแล้วกระบวนการค้นหาจำนวนนิวตรอนจะเหมือนกับที่ใช้กับอะตอมธรรมดา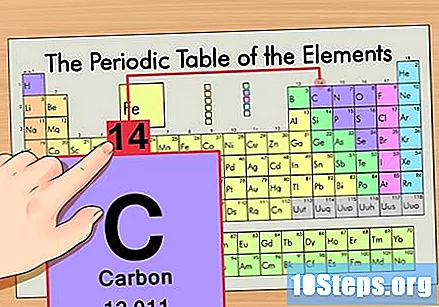
ลบเลขอะตอมออกจากมวลอะตอม เนื่องจากมวลส่วนใหญ่ของอะตอมพบในโปรตอนและนิวตรอนการลบจำนวนโปรตอน (นั่นคือเลขอะตอม) ออกจากมวลอะตอมจะทำให้คุณได้จำนวน คำนวณ ของนิวตรอนในอะตอม โดยทั่วไปแล้วจำนวนหลังจุดทศนิยมจะแสดงถึงมวลของอิเล็กตรอนที่มีขนาดเล็กมากในอะตอม ในตัวอย่างของเรานี่คือ 14 (มวลอะตอม) - 6 (จำนวนโปรตอน) = 8 (จำนวนนิวตรอน)
จำสูตร. หากต้องการหาจำนวนนิวตรอนในอนาคตให้ใช้สูตรนี้: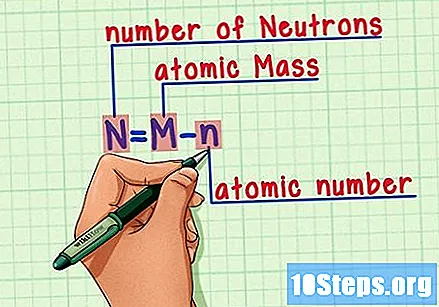
- N = M - น.
- N = จำนวน ยังไม่มีข้อความeutrons
- M = Mปรมาณูย่าง.
- n = nกระดูกต้นแขน
- N = M - น.
เคล็ดลับ
- Osmium ซึ่งเป็นโลหะแข็งที่อุณหภูมิห้องมีที่มาจากคำภาษากรีกสำหรับ 'กลิ่น', 'osme'
- โปรตอนและนิวตรอนประกอบขึ้นเป็นน้ำหนักเกือบทั้งหมดขององค์ประกอบในขณะที่อิเล็กตรอนและอนุภาคอื่น ๆ ที่มีความหลากหลายเป็นตัวแทนของมวลเล็กน้อย (เข้าใกล้มวลเป็นศูนย์) เนื่องจากโปรตอนมีน้ำหนักเท่ากับเป็นกลางและเลขอะตอมแทนจำนวนโปรตอนเราจึงสามารถลบจำนวนโปรตอนออกจากมวลทั้งหมดได้
- หากคุณไม่แน่ใจว่าตัวเลขใดอยู่ในตารางธาตุโปรดจำไว้ว่าโดยปกติแล้วจะสร้างขึ้นรอบเลขอะตอม (นั่นคือจำนวนโปรตอน) ซึ่งเริ่มต้นด้วย 1 (ไฮโดรเจน) และเพิ่มขึ้นหนึ่งหน่วยต่อ จากซ้ายไปขวาลงท้ายด้วย 118 (Ununóctio) เนื่องจากจำนวนโปรตอนในอะตอมเป็นตัวกำหนดว่าอะตอมนั้นคืออะไรทำให้เอื้อต่อการจัดองค์ประกอบของลักษณะธาตุ (ตัวอย่างเช่นอะตอมที่มีโปรตอน 2 ตัวจะเป็นฮีเลียมเสมอเช่นเดียวกับอะตอมอื่นที่มีโปรตอน 79 ตัวจะเป็นทองคำเสมอ)