เนื้อหา
ในบทความนี้: สมดุลสมการโดยวิธีการทดลองและข้อผิดพลาดสมดุลสมการโดยวิธีพีชคณิตสรุปของบทความอ้างอิง
ในทางเคมีสมการจะกำหนดสิ่งที่เกิดขึ้นระหว่างปฏิกิริยาทางเคมี ทางด้านซ้ายของสมการเราวางรีเอเจนต์ที่ใช้สำหรับการทดลองและด้านขวาคือผลิตภัณฑ์ที่ได้จากการทดลอง ตามหลักการของการอนุรักษ์มวล (Lavoisier) ในระหว่างการทำปฏิกิริยาเคมีไม่มีอะตอมหายไปไม่มีการสร้างพวกเขารวมกันแตกต่างกัน โดยสรุปคุณจะต้องมีข้อมูลจำนวนเท่ากันของแต่ละองค์ประกอบทางด้านขวาเหมือนกับด้านซ้ายของสมการ นั่นคือเหตุผลที่สมการสมดุลต้องสมดุลเสมอ
ขั้นตอน
วิธีที่ 1 สร้างสมดุลของสมการโดยการลองผิดลองถูก
-
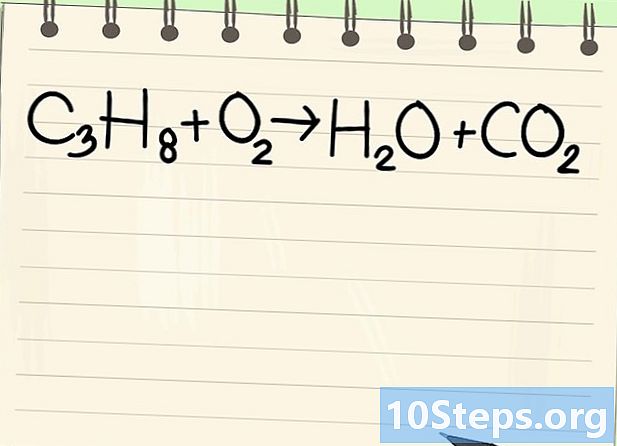
จดบันทึกสมการสมดุล เราจะปฏิบัติต่อสมการต่อไปนี้:- C3H8 + O2 -> ชั่วโมง2O + CO2
- นี่คือสมการการเผาไหม้โพรเพน (C)3H8) ในออกซิเจน: ได้รับน้ำและคาร์บอนไดออกไซด์
-
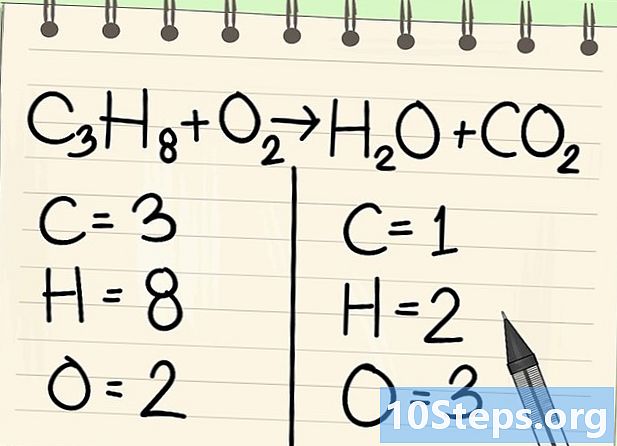
นับอะตอม ป้อนจำนวนของชุดข้อมูลของแต่ละองค์ประกอบในด้านหนึ่งของสมการแล้วอีกชุดหนึ่ง สำหรับเรื่องนี้ให้คำนึงถึงดัชนีหากไม่มีดัชนีก็คือ 1- ทางซ้ายมีอะตอมคาร์บอน 3 ตัวคือ 8 ไฮโดรเจนและออกซิเจน 2 ตัว
- ด้านขวามีคาร์บอน 1 อะตอม 2 ไฮโดรเจนและออกซิเจน 3 อะตอม
-
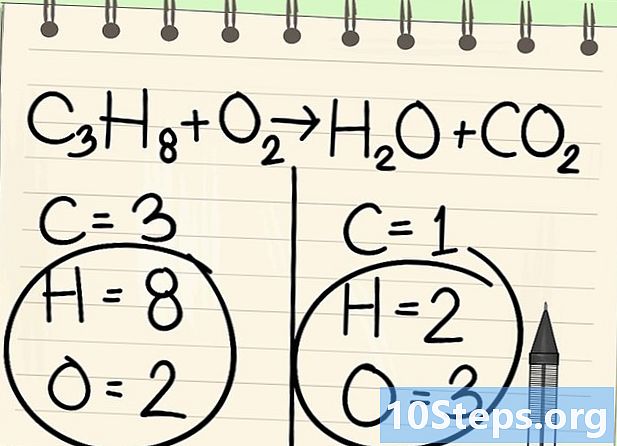
ทิ้งไฮโดรเจนและออกซิเจนไว้ชั่วคราว -

เริ่มปรับสมดุลด้วยองค์ประกอบที่เหมาะสม เรามักจะเริ่มต้นด้วยหนึ่งในโมเลกุลก่อนและหลังปฏิกิริยา หากมีหลายให้ใช้หนึ่งที่ monovalent ในหนึ่งในโมเลกุล ที่นี่เราเริ่มต้นด้วยอะตอมคาร์บอน -

ปรับสมดุลของอะตอมคาร์บอน เพิ่มทางขวาสัมประสิทธิ์ของโมเลกุลคาร์บอนไดออกไซด์ (CO.)2) ซึ่ง Latome ของคาร์บอนอยู่คนเดียว เราจะใส่ 3 เพื่อให้ได้ 3 อะตอมที่เหลือ- C3H8 + O2 -> ชั่วโมง2O + 3CO2
- เรามีคาร์บอน 3 อะตอมทางด้านขวาด้วยค่าสัมประสิทธิ์ (3CO)2) และ 3 อะตอมคาร์บอนทางด้านซ้ายด้วยดัชนี (C3H8).
- ในสมการคุณสามารถใส่สัมประสิทธิ์ทั้งหมดที่คุณต้องการ แต่คุณไม่สามารถสัมผัสเบาะแสได้
-
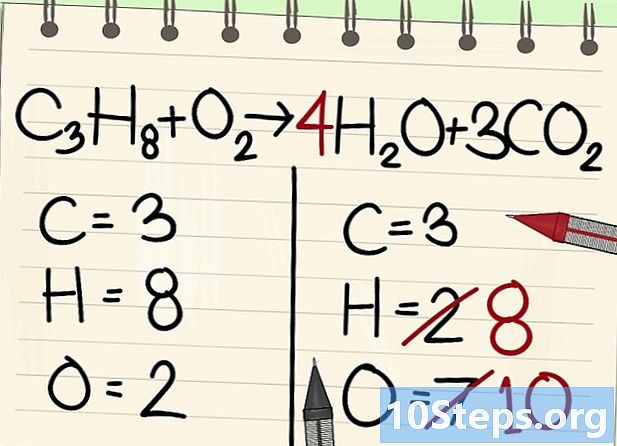
ปรับสมดุลอะตอมไฮโดรเจน เนื่องจากคุณมี 8 เหลืออยู่ของสมการคุณจึงต้องถูกต้องมาก- C3H8 + O2 --> 4H2O + 3CO2
- ทางด้านขวาคุณจะใส่ค่าสัมประสิทธิ์เป็น 4 เพราะไฮโดรเจนเป็นไบวาเลนซ์ในโมเลกุลของน้ำ: ดัชนี 2 บ่งชี้ว่าอะตอมไฮโดรเจนสองอันเกี่ยวข้อง
- ในการรับจำนวนอะตอมไฮโดรเจนทางขวาคุณคูณสัมประสิทธิ์ 4 ด้วยดัชนี 2 หรือ 8 อะตอม
- สำหรับอะตอมของออกซิเจนทางด้านขวาตอนนี้มี 6 ด้านหนึ่งมาจากสามโมเลกุลของ 3CO2 (3 x 2 = 6 อะตอม) และ 4 จาก 4 โมเลกุล 4 ชั่วโมง2O (4 x 1 = 4 อะตอม) คือจำนวนออกซิเจน 10 อะตอม
-
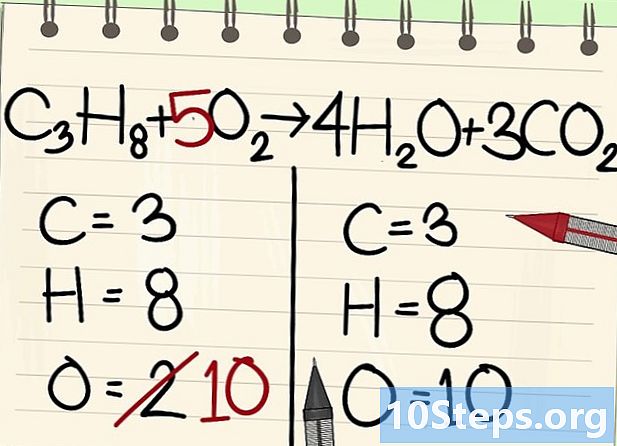
ปรับสมดุลอะตอมของออกซิเจน- เนื่องจากความสมดุลของคาร์บอนและไฮโดรเจนจำนวนอะตอมออกซิเจนไม่เท่ากันทั้งสองด้านของสมการ ก่อนหน้านี้เราเห็นว่ามีออกซิเจน 10 อะตอมทางด้านขวา (4 จากโมเลกุลน้ำและ 6 จากโมเลกุลคาร์บอนไดออกไซด์) ด้านซ้ายมีเพียง 2 (จาก O2).
- เพื่อเพิ่มความสมดุลของออกซิเจนให้เพิ่มค่าสัมประสิทธิ์ 5 ไปที่โมเลกุลออกซิเจนด้านซ้าย: คุณมีออกซิเจน 10 อะตอมทางซ้ายและอีกอันอยู่ทางขวา
- C3H8 + 5O2 -> 4H2O + 3CO2
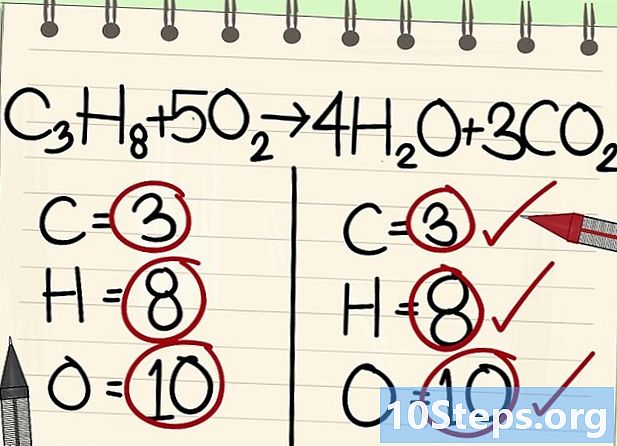
- อะตอมทั้งหมด (คาร์บอนไฮโดรเจนและออกซิเจน) มีความสมดุลสมการของคุณมีความสมดุล
วิธีที่ 2 ปรับสมดุลสมการด้วยวิธีพีชคณิต
-

เขียนสมการเพื่อความสมดุล กำหนดแต่ละค่าสัมประสิทธิ์ของตัวอักษร เราจะเรียกพวกเขาว่า มี, ข, ค และ d. -
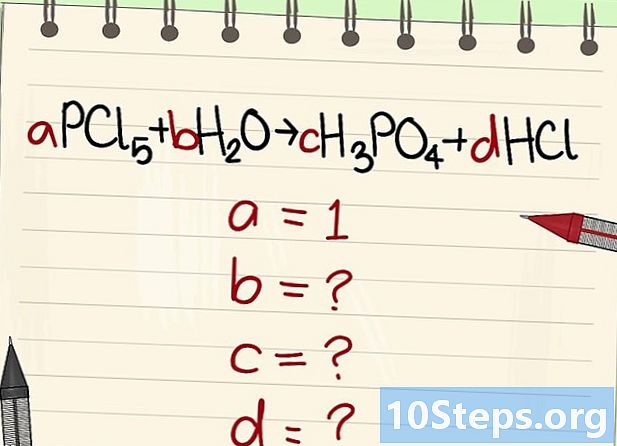
ค้นหาค่าของสัมประสิทธิ์ตัวอักษรอื่น ๆ เราจะถามว่า มี = 1. -

ค้นหาความสัมพันธ์ระหว่างค่าสัมประสิทธิ์เหล่านี้ มองไปทางซ้าย (รีเอเจนต์) และขวา (ผลิตภัณฑ์) สร้างความสัมพันธ์ระหว่างค่าสัมประสิทธิ์ที่แตกต่างกันเหล่านี้- ใช้สมการต่อไปนี้: aPCl5 + bH2O = cH3PO4 + dHCl มันได้รับการระบุว่า a = 1 ซึ่งหมายความว่า c = a, d = 5a และ 2b = 3c + d คำนวณเสร็จแล้ว c = 1, d = 5 และ b = 4

- ใช้สมการต่อไปนี้: aPCl5 + bH2O = cH3PO4 + dHCl มันได้รับการระบุว่า a = 1 ซึ่งหมายความว่า c = a, d = 5a และ 2b = 3c + d คำนวณเสร็จแล้ว c = 1, d = 5 และ b = 4