เนื้อหา
ในทางเคมี "ความดันบางส่วน" หมายถึงความดันที่ก๊าซแต่ละชนิดในส่วนผสมของก๊าซกระทำต่อสิ่งรอบข้างเช่นขวดตัวอย่างถังอากาศดำน้ำหรือขีด จำกัด ของบรรยากาศ คุณสามารถคำนวณความดันของก๊าซแต่ละชนิดในส่วนผสมได้หากคุณทราบว่ามีปริมาณเท่าใดปริมาตรเท่าใดและมีอุณหภูมิเท่าใด จากนั้นคุณสามารถเพิ่มแรงกดดันบางส่วนเหล่านี้เพื่อหาความดันรวมของส่วนผสมของก๊าซหรือคุณสามารถหาค่าความดันรวมก่อนแล้วจึงหาแรงดันบางส่วน
ขั้นตอน
ส่วนที่ 1 ของ 3: การทำความเข้าใจคุณสมบัติของก๊าซ
ถือว่าก๊าซแต่ละชนิดเป็นก๊าซ "อุดมคติ" ก๊าซในอุดมคติในทางเคมีคือก๊าซที่ทำปฏิกิริยากับก๊าซอื่น ๆ โดยไม่ถูกดึงดูดเข้าสู่โมเลกุลของมัน โมเลกุลแต่ละโมเลกุลสามารถตีกันและกระเด็นออกไปเหมือนลูกบิลเลียดโดยไม่ผิดรูป แต่อย่างใด
- ความกดดันของก๊าซในอุดมคติจะเพิ่มขึ้นเมื่อถูกบีบอัดลงในช่องว่างขนาดเล็กและลดลงเมื่อขยายเข้าไปในพื้นที่ขนาดใหญ่ ความสัมพันธ์นี้เรียกว่ากฎของบอยล์หลังจากโรเบิร์ตบอยล์ มีการอธิบายทางคณิตศาสตร์ว่า k = P x V หรือพูดง่ายๆก็คือ k = PV โดยที่ k หมายถึงความสัมพันธ์คงที่ P หมายถึงความดันและ V แทนปริมาตร
- ความกดดันสามารถกำหนดได้โดยใช้หน่วยใดหน่วยหนึ่งที่เป็นไปได้ หนึ่งคือ Pascal (Pa) ซึ่งหมายถึงแรงนิวตันที่กระทำในตารางเมตร อีกประการหนึ่งคือบรรยากาศ (atm) ซึ่งหมายถึงความกดดันของบรรยากาศโลกที่ระดับน้ำทะเล ความดัน 1 atm เท่ากับ 101,325 Pa
- อุณหภูมิของก๊าซในอุดมคติจะเพิ่มขึ้นเมื่อปริมาณเพิ่มขึ้นและลดลง ความสัมพันธ์นี้เรียกว่ากฎของชาร์ลส์ตามหลัง Jacques Charles และอธิบายทางคณิตศาสตร์ว่า k = V / t โดยที่ k แสดงถึงความสัมพันธ์ระหว่างปริมาตรและอุณหภูมิคงที่ V หมายถึงปริมาตรอีกครั้งและ T หมายถึงอุณหภูมิ
- อุณหภูมิของก๊าซในสมการนี้กำหนดเป็นองศาเคลวินซึ่งพบได้จากการเพิ่ม 273 เป็นจำนวนองศาเซลเซียสของอุณหภูมิก๊าซ
- ความสัมพันธ์ทั้งสองนี้สามารถรวมกันเป็นสมการเดียว: k = PV / T ซึ่งสามารถเขียนเป็น PV = kT ได้

กำหนดปริมาณก๊าซที่วัดได้ ก๊าซมีมวลและปริมาตร โดยปกติปริมาตรจะวัดเป็นลิตร (l) แต่มีมวลสองประเภท- มวลทั่วไปจะวัดเป็นกรัมหรือถ้ามีมวลมากพอก็กิโลกรัม
- เนื่องจากความเบาของก๊าซจึงวัดในมวลรูปแบบอื่นที่เรียกว่ามวลโมเลกุลหรือมวลโมลาร์ มวลโมลาร์หมายถึงผลรวมของน้ำหนักอะตอมของแต่ละอะตอมของสารประกอบที่สร้างก๊าซโดยแต่ละอะตอมเปรียบเทียบกับค่า 12 สำหรับคาร์บอน
- เนื่องจากอะตอมและโมเลกุลมีขนาดเล็กเกินไปที่จะทำงานได้ปริมาณของก๊าซจึงถูกกำหนดเป็นโมล จำนวนโมลที่มีอยู่ในก๊าซหนึ่ง ๆ สามารถกำหนดได้โดยการหารมวลด้วยมวลโมลาร์และสามารถแทนด้วยตัวอักษร n
- เราสามารถแทนที่ค่าคงที่โดยพลการ k ในสมการของแก๊สด้วยผลคูณของ n จำนวนโมล (โมล) และค่าคงที่ใหม่ R ขณะนี้สามารถเขียนสมการได้ nR = PV / T หรือ PV = nRT
- ค่า R ขึ้นอยู่กับหน่วยที่ใช้ในการวัดความดันปริมาตรและอุณหภูมิของก๊าซ ในการระบุปริมาตรเป็นลิตรอุณหภูมิในหน่วยเคลวินและความดันในบรรยากาศค่าของมันคือ 0.0821 L.atm / K.mol นอกจากนี้ยังสามารถเขียน L 0.0821 atm K mol เพื่อหลีกเลี่ยงแถบแยกในหน่วยการวัด

ทำความเข้าใจกฎแห่งแรงกดดันบางส่วนของดาลตัน พัฒนาโดยนักเคมีและนักฟิสิกส์จอห์นดาลตันซึ่งเป็นคนแรกที่พัฒนาแนวคิดเรื่ององค์ประกอบทางเคมีที่สร้างจากอะตอมกฎของดอลตันระบุว่าความดันรวมของส่วนผสมของก๊าซคือผลรวมของความกดดันของก๊าซแต่ละชนิดในส่วนผสม- กฎของดาลตันสามารถเขียนเป็นสมการเป็น P รวม = ป1 + ป2 + ป3... มีภาคผนวกหลังเครื่องหมายเท่ากับมากที่สุดเท่าที่มีก๊าซอยู่ในส่วนผสม
- สมการกฎของดาลตันสามารถขยายได้เมื่อทำงานกับก๊าซที่ไม่ทราบแรงกดดันบางส่วนของแต่ละบุคคล แต่เราทราบปริมาตรและอุณหภูมิของมัน ความดันบางส่วนของก๊าซมีความดันเท่ากันถ้าก๊าซในปริมาณเท่ากันเป็นก๊าซชนิดเดียวในภาชนะ
- สำหรับความกดดันบางส่วนเราสามารถเขียนสมการของก๊าซในอุดมคติใหม่เพื่อที่ในแทนที่จะเป็นสูตร PV = nRT เราจะมี P ได้เพียงทางด้านซ้ายของเครื่องหมายเท่ากับ ในการทำเช่นนี้เราหารทั้งสองข้างด้วย V: PV / V = nRT / V ทั้งสอง Vs ทางด้านซ้ายจะยกเลิกซึ่งกันและกันโดยปล่อยให้ P = nRT / V
- จากนั้นเราสามารถแทนที่แต่ละ P ที่สมัครไว้ทางด้านขวาของสมการความดันบางส่วน: Pรวม = (nRT / V) 1 + (nRT / V) 2 + (nRT / V) 3…
ส่วนที่ 2 จาก 3: การคำนวณแรงกดดันบางส่วนและความกดดันทั้งหมด

กำหนดสมการความดันบางส่วนสำหรับก๊าซที่คุณกำลังใช้งาน สำหรับวัตถุประสงค์ในการคำนวณนี้เราจะถือว่าบอลลูนขนาด 2 ลิตรบรรจุก๊าซสามตัว: ไนโตรเจน (N2), ออกซิเจน (O2) และคาร์บอนไดออกไซด์ (CO2). ก๊าซแต่ละชนิดมี 10 กรัมและอุณหภูมิของก๊าซแต่ละชนิดในขวดคือ37ºเซลเซียส เราต้องหาความดันบางส่วนของก๊าซแต่ละชนิดและความดันรวมที่ส่วนผสมกระทำต่อภาชนะบรรจุ- สมการความดันบางส่วนของเรากลายเป็น P รวม = ป ไนโตรเจน + ป ออกซิเจน + ป คาร์บอนไดออกไซด์ .
- เนื่องจากเราพยายามค้นหาความดันที่ก๊าซแต่ละตัวออกแรงเราจึงทราบปริมาตรและอุณหภูมิและเราสามารถหาจำนวนโมลของก๊าซแต่ละตัวตามมวลเราจึงสามารถเขียนสมการนี้ใหม่เป็น: Pรวม = (nRT / V) ไนโตรเจน + (nRT / V) ออกซิเจน + (nRT / V) คาร์บอนไดออกไซด์

แปลงอุณหภูมิเป็นเคลวิน อุณหภูมิ37ºเซลเซียสเพิ่ม 273 ถึง 37 เพื่อให้ได้ 310 K
ค้นหาจำนวนโมลของก๊าซแต่ละตัวในตัวอย่าง จำนวนโมลของก๊าซคือมวลของก๊าซที่หารด้วยมวลโมลาร์ซึ่งเรากล่าวว่าเป็นผลรวมของน้ำหนักอะตอมของแต่ละอะตอมในสารประกอบ
- สำหรับก๊าซแรกไนโตรเจน (N2) แต่ละอะตอมมีน้ำหนักอะตอมเท่ากับ 14 เนื่องจากไนโตรเจนเป็นไดอะตอมมิก (รูปแบบโมเลกุลของสองอะตอม) เราจึงต้องคูณ 14 ด้วย 2 จึงจะพบว่าไนโตรเจนในตัวอย่างของเรามีมวลโมลาร์เท่ากับ 28 จากนั้นจึงแบ่งมวล ในหน่วยกรัม 10 กรัมคูณ 28 เพื่อให้ได้จำนวนโมลซึ่งเราจะได้ไนโตรเจนประมาณ 0.4 โมล
- สำหรับก๊าซที่สองออกซิเจน (O2) แต่ละอะตอมมีน้ำหนักอะตอมเท่ากับ 16 ออกซิเจนก็เป็นไดอะตอมเช่นกันดังนั้นจงคูณ 16 ด้วย 2 จะพบว่าออกซิเจนในตัวอย่างมีมวลโมลาร์ 32 การหาร 10 ก. ด้วย 32 จะทำให้เรามีออกซิเจนประมาณ 0.3 โมลในตัวเรา ตัวอย่าง.
- ก๊าซที่สามคาร์บอนไดออกไซด์ (CO2) มี 3 อะตอม: หนึ่งคาร์บอนน้ำหนักอะตอม 12; และออกซิเจนสองตัวแต่ละตัวมีน้ำหนักอะตอมเท่ากับ 16 เราเพิ่มน้ำหนักสามตัว: 12 + 16 + 16 = 44 สำหรับมวลโมลาร์ การหาร 10 ก. ด้วย 44 จะทำให้เรามีคาร์บอนไดออกไซด์ประมาณ 0.2 โมล

แทนที่ค่าด้วยโมลปริมาตรและอุณหภูมิ ตอนนี้สมการของเรามีลักษณะดังนี้: Pรวม = (0.4 * R * 310/2) ไนโตรเจน + (0.3 * R * 310/2) ออกซิเจน + (0.2 * R * 310/2) คาร์บอนไดออกไซด์.- เพื่อความง่ายเราได้ละเว้นหน่วยการวัดที่มาพร้อมกับค่า หน่วยเหล่านี้จะถูกยกเลิกหลังจากที่เราทำคณิตศาสตร์แล้วเหลือเพียงหน่วยวัดที่เราใช้ในการรายงานแรงกดดัน
แทนค่าสำหรับค่าคงที่ R เราจะพบความกดดันบางส่วนและทั้งหมดในชั้นบรรยากาศดังนั้นเราจะใช้ค่า R ที่ 0.0821 atm L / K.mol การแทนค่าในสมการตอนนี้ทำให้เราได้ Pรวม =(0,4 * 0,0821 * 310/2) ไนโตรเจน + (0,3 *0,0821 * 310/2) ออกซิเจน + (0,2 * 0,0821 * 310/2) คาร์บอนไดออกไซด์ .
คำนวณแรงดันบางส่วนสำหรับแต่ละก๊าซ ตอนนี้เรามีค่าเข้าที่แล้วก็ถึงเวลาคำนวณ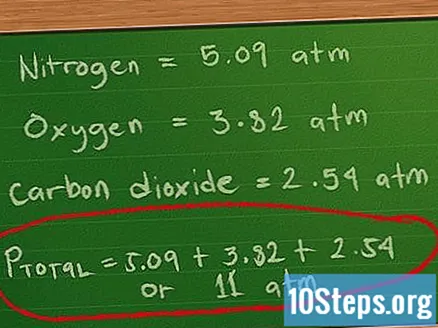
- สำหรับความดันบางส่วนของไนโตรเจนเราคูณ 0.4 โมลด้วยค่าคงที่ 0.0821 และอุณหภูมิ 310 K ของเราแล้วหารด้วย 2 ลิตร: 0.4 * 0.0821 * 310/2 = 5, 09 atm โดยประมาณ
- สำหรับความดันออกซิเจนบางส่วนเราคูณ 0.3 โมลด้วยค่าคงที่ 0.0821 และอุณหภูมิ 310 K ของเราแล้วหารด้วย 2 ลิตร: 0.3 * 0.0821 * 310/2 = 3, 82 atm โดยประมาณ
- สำหรับความดันบางส่วนของคาร์บอนไดออกไซด์เราคูณ 0.2 โมลด้วยค่าคงที่ 0.0821 และอุณหภูมิ 310 K ของเราแล้วหารด้วย 2 ลิตร: 0.2 * 0.0821 * 310/2 = 2.54 atm โดยประมาณ
- ตอนนี้เราเพิ่มแรงกดดันเหล่านี้เพื่อค้นหาความดันทั้งหมด: Pรวม = 5.09 + 3.82 + 2.54 หรือประมาณ 11.45 atm
ส่วนที่ 3 ของ 3: การคำนวณความดันรวมและความดันบางส่วน
กำหนดสมการความดันบางส่วนเหมือนเดิม อีกครั้งเราคิดว่าขวดขนาด 2 ลิตรมี 3 ก๊าซ: ไนโตรเจน (N2), ออกซิเจน (O2) และคาร์บอนไดออกไซด์ (CO2). ก๊าซแต่ละชนิดมีอยู่ 10 กรัมและอุณหภูมิของก๊าซแต่ละชนิดในขวดคือ 37 องศาเซลเซียส
- อุณหภูมิในเคลวินจะยังคงเป็น 310 และเช่นเดิมเรามีไนโตรเจนประมาณ 0.4 โมลออกซิเจน 0.3 โมลและคาร์บอนไดออกไซด์ 0.2 โมล
- ในทำนองเดียวกันเราจะยังคงพบความกดดันในบรรยากาศดังนั้นเราจะใช้ค่า 0.0821 atm L / K.mol สำหรับค่าคงที่ R
- ดังนั้นสมการความดันบางส่วนของเรายังคงเหมือนเดิม ณ จุดนี้: Pรวม =(0,4 * 0,0821 * 310/2) ไนโตรเจน + (0,3 *0,0821 * 310/2) ออกซิเจน + (0,2 * 0,0821 * 310/2) คาร์บอนไดออกไซด์.
เพิ่มจำนวนโมลของก๊าซแต่ละตัวในตัวอย่างเพื่อหาจำนวนโมลทั้งหมดของส่วนผสมของก๊าซ เนื่องจากปริมาตรและอุณหภูมิเหมือนกันสำหรับแต่ละตัวอย่างในก๊าซจึงไม่ต้องพูดถึงว่าค่าโมลาร์แต่ละค่าจะถูกคูณด้วยค่าคงที่เท่ากันเราจึงสามารถใช้คุณสมบัติการกระจายของคณิตศาสตร์เพื่อเขียนสมการใหม่เป็น Pรวม = (0,4 + 0,3 + 0,2) * 0,0821 * 310/2.
- การเพิ่ม 0.4 + 0.3 + 0.2 = 0.9 โมลของส่วนผสมของก๊าซ สิ่งนี้จะทำให้สมการของ P ง่ายขึ้น รวม = 0,9 * 0,0821 * 310/2.
คำนวณความดันรวมของส่วนผสมของก๊าซ การคูณ 0.9 * 0.0821 * 310/2 = 11.45 โมลโดยประมาณ
หาสัดส่วนของก๊าซแต่ละชนิดในส่วนผสมทั้งหมด ในการทำเช่นนี้ให้หารจำนวนโมลสำหรับแต่ละก๊าซด้วยจำนวนโมลทั้งหมด
- มีไนโตรเจน 0.4 โมลดังนั้น 0.4 / 0.9 = 0.44 (44%) ของตัวอย่างโดยประมาณ
- มีไนโตรเจน 0.3 โมลดังนั้น 0.3 / 0.9 = 0.33 (33%) ของตัวอย่างโดยประมาณ
- มีคาร์บอนไดออกไซด์ 0.2 โมลดังนั้น 0.2 / 0.9 = 0.22 (22%) ของตัวอย่างประมาณ
- แม้ว่าเปอร์เซ็นต์โดยประมาณข้างต้นจะรวมกันได้เพียง 0.99 แต่ทศนิยมที่แท้จริงจะเกิดซ้ำดังนั้นผลรวมที่แท้จริงจึงเป็นชุดของการทำซ้ำของเก้าหลังจุดทศนิยม ตามความหมายนี่เหมือนกับ 1 หรือ 100%
คูณค่าสัดส่วนของแต่ละก๊าซด้วยความดันทั้งหมดเพื่อหาความดันบางส่วน
- การคูณ 0.44 * 11.45 = 5.04 atm โดยประมาณ
- การคูณ 0.33 * 11.45 = 3.78 atm โดยประมาณ
- การคูณ 0.22 * 11.45 = 2.52 atm โดยประมาณ
เคล็ดลับ
- คุณจะสังเกตเห็นความแตกต่างเล็กน้อยของค่าโดยการหาค่าความดันบางส่วนก่อนจากนั้นจึงหาค่าความดันทั้งหมดและค้นหาความดันรวมก่อนแล้วจึงค่อยหาค่าความดันบางส่วน โปรดจำไว้ว่าค่าที่ระบุถูกนำเสนอเป็นค่าโดยประมาณเนื่องจากการปัดเศษเป็นทศนิยมหนึ่งหรือสองตำแหน่งเพื่อให้เข้าใจค่าได้ง่ายขึ้น หากคุณทำการคำนวณด้วยเครื่องคิดเลขโดยไม่ต้องปัดเศษคุณจะสังเกตเห็นความคลาดเคลื่อนเล็กน้อยระหว่างสองวิธีหากมี
คำเตือน
- ความรู้เกี่ยวกับแรงดันก๊าซบางส่วนอาจกลายเป็นเรื่องของชีวิตและความตายสำหรับนักดำน้ำ ความดันออกซิเจนบางส่วนที่ต่ำเกินไปอาจทำให้หมดสติและเสียชีวิตได้ในขณะที่ความดันไฮโดรเจนหรือออกซิเจนบางส่วนที่สูงมากก็อาจเป็นพิษได้เช่นกัน
วัสดุที่จำเป็น
- เครื่องคิดเลข;
- หนังสืออ้างอิงน้ำหนักอะตอม / มวลโมลาร์.