เนื้อหา
มวลเปอร์เซ็นต์กำหนดเปอร์เซ็นต์ของแต่ละองค์ประกอบที่เป็นสารประกอบทางเคมี ในการหาค่านี้คุณจะต้องมีมวลโมลาร์ขององค์ประกอบสารประกอบเป็นกรัม / โมลหรือจำนวนกรัมที่ใช้ในการสร้างสารละลาย มวลเปอร์เซ็นต์สามารถคำนวณได้ด้วยวิธีง่ายๆโดยใช้สูตรพื้นฐานที่แบ่งมวลขององค์ประกอบ (หรือตัวถูกละลาย) ด้วยมวลของสารประกอบ (หรือสารละลาย)
ขั้นตอน
วิธีที่ 1 จาก 2: การหามวลเปอร์เซ็นต์ด้วยมวลที่กำหนด
- กำหนดสมการสำหรับมวลเปอร์เซ็นต์ของสารประกอบ สูตรพื้นฐานสำหรับสารประกอบคือเปอร์เซ็นต์มวล = () x 100 คุณต้องคูณผลลัพธ์ด้วย 100 ในตอนท้ายเพื่อแสดงค่าเป็นเปอร์เซ็นต์
- มวลของสารประกอบทางเคมีที่คุณสนใจคือมวลที่กำหนดในโจทย์ หากไม่ได้ระบุค่านี้ให้อ้างอิงวิธีการต่อไปนี้และเรียนรู้วิธีการหามวลเปอร์เซ็นต์เมื่อไม่ได้กำหนดมวล
- มวลรวมของสารประกอบคำนวณโดยการเพิ่มมวลขององค์ประกอบทั้งหมดที่ใช้สร้างสารประกอบหรือสารละลาย
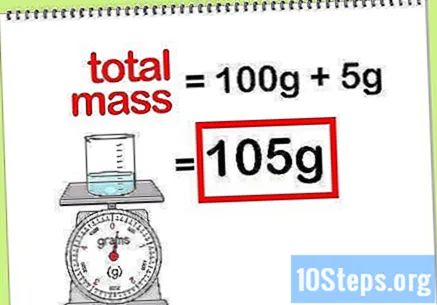
คำนวณมวลรวมของสารประกอบ เมื่อคุณทราบค่ามวลของธาตุหรือสารประกอบทั้งหมดที่เพิ่มเข้ามาคุณก็ต้องบวกมันเพื่อคำนวณมวลของสารประกอบหรือวิธีแก้ปัญหาสุดท้าย ค่านี้จะเป็นตัวหารในการคำนวณมวลเปอร์เซ็นต์- ตัวอย่างเช่น: โซเดียมไฮดรอกไซด์ 5 กรัมละลายในน้ำ 100 กรัมมีมวลกี่เปอร์เซ็นต์?
- มวลรวมของสารประกอบคือปริมาณโซเดียมเปอร์ออกไซด์บวกปริมาณน้ำ: 100 ก. + 5 ก. รวมมวล 105 ก.

ระบุมวลของสารเคมีที่เป็นปัญหา เมื่อคุณต้องการค้นหาไฟล์ มวลเปอร์เซ็นต์ปัญหาต้องการให้คุณหามวลขององค์ประกอบเฉพาะ (องค์ประกอบที่เป็นปัญหา) เป็นเปอร์เซ็นต์ของมวลรวมขององค์ประกอบทั้งหมด สังเกตมวลขององค์ประกอบที่เป็นปัญหา ค่านี้จะเป็นตัวเศษในการคำนวณมวลเปอร์เซ็นต์- ตัวอย่างเช่นมวลของธาตุคือโซเดียมไฮดรอกไซด์ 5 กรัม
- แทนตัวแปรในสูตรมวลเปอร์เซ็นต์ หลังจากกำหนดค่าสำหรับแต่ละตัวแปรแล้วให้แทนที่ในสมการ
- ตัวอย่างเช่นมวลเปอร์เซ็นต์ = () x 100 = () x 100

คำนวณมวลเปอร์เซ็นต์ ตอนนี้สมการถูกสร้างขึ้นแล้วเพียงแค่แก้มันเพื่อคำนวณมวลเปอร์เซ็นต์ หารมวลของธาตุด้วยมวลรวมของสารประกอบแล้วคูณด้วย 100 ผลลัพธ์ที่ได้จะเป็นมวลเปอร์เซ็นต์ขององค์ประกอบทางเคมี- ตัวอย่างเช่น: () x 100 = 0.04761 x 100 = 4.751% ดังนั้นเปอร์เซ็นต์มวลของโซเดียมไฮดรอกไซด์ 5 กรัมที่ละลายในน้ำ 100 กรัมจึงเท่ากับ 4.751%
วิธีที่ 2 จาก 2: การหามวลเปอร์เซ็นต์ที่ไม่มีมวล
- กำหนดสมการสำหรับมวลเปอร์เซ็นต์ของสารประกอบ สูตรพื้นฐานสำหรับมวลเปอร์เซ็นต์ของสารประกอบคือ: มวลเปอร์เซ็นต์ = () x 100 คุณต้องคูณผลลัพธ์ด้วย 100 ในตอนท้ายเพื่อแสดงค่าเป็นเปอร์เซ็นต์
- เมื่อคุณไม่ทราบค่ามวลคุณสามารถหาเปอร์เซ็นต์มวลขององค์ประกอบของสารประกอบโดยใช้มวลโมลาร์
- ตัวอย่างเช่น: มวลเปอร์เซ็นต์ของไฮโดรเจนในโมเลกุลของน้ำคืออะไร?.
เขียน สูตรเคมี. หากไม่ได้ระบุสูตรทางเคมีสำหรับสารประกอบแต่ละชนิดคุณจะต้องจดไว้ มิฉะนั้นให้ข้ามไปที่ขั้นตอน "ค้นหามวลของแต่ละองค์ประกอบ"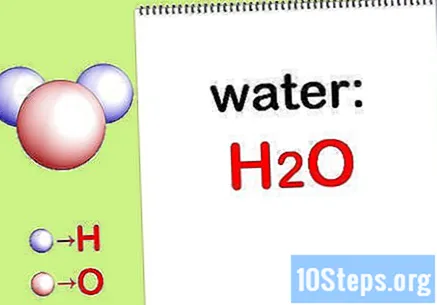
- ตัวอย่างเช่นเขียนสูตรเคมีของน้ำ: H2เดอะ.
หามวลของแต่ละองค์ประกอบในสารประกอบ มองหาน้ำหนักโมเลกุลของแต่ละองค์ประกอบของสูตรเคมีโดยอ้างอิงจากตารางธาตุ โดยทั่วไปมวลขององค์ประกอบจะอยู่ด้านล่างสัญลักษณ์องค์ประกอบทางเคมี สังเกตมวลของแต่ละองค์ประกอบของสารประกอบ
- ตัวอย่างเช่นมวลโมเลกุลของออกซิเจนเท่ากับ 15.9994 และไฮโดรเจนเท่ากับ 1.0079
คูณมวลด้วยอัตราส่วนโมลาร์ ระบุจำนวนโมลของแต่ละองค์ประกอบในสารประกอบทางเคมี จำนวนโมลจะได้รับจากจำนวนที่สมัครของสารประกอบ คูณมวลโมเลกุลของแต่ละองค์ประกอบด้วยอัตราส่วนโมลาร์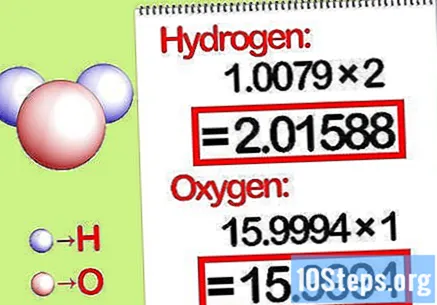
- ตัวอย่างเช่นอัตราส่วนโมลาร์ของไฮโดรเจนต่อออกซิเจนในน้ำคือ 2: 1 ดังนั้นให้คูณน้ำหนักโมเลกุลของไฮโดรเจนด้วยสอง (1.00794 X 2 = 2.01588) และปล่อยให้น้ำหนักโมเลกุลของออกซิเจนตามที่เป็น (15.9994)
คำนวณมวลรวมของสารประกอบ เพิ่มมวลรวมขององค์ประกอบทั้งหมดของสารประกอบ การใช้มวลที่คำนวณโดยอัตราส่วนโมลาร์ทำให้สามารถคำนวณมวลรวมของสารประกอบได้ ตัวเลขนี้จะเป็นตัวส่วนของสมการมวลเปอร์เซ็นต์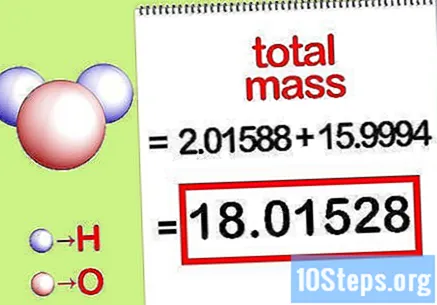
- ตัวอย่างเช่นเพิ่ม 2.01588 g / mol (มวลของอะตอมไฮโดรเจน 2 โมล) ด้วย 15.9994 g / mol (มวลของอะตอมออกซิเจน 1 โมล) และได้ 18.01528 g / mol
ระบุมวลขององค์ประกอบที่เป็นปัญหา เมื่อคุณต้องการค้นหาไฟล์ มวลเปอร์เซ็นต์โจทย์ต้องการให้คุณหามวลขององค์ประกอบเฉพาะในสารประกอบเป็นเปอร์เซ็นต์ของมวลรวมขององค์ประกอบทั้งหมด ระบุมวลขององค์ประกอบที่เป็นปัญหาและจดไว้ เป็นค่ามวลที่คำนวณโดยใช้อัตราส่วนโมลาร์ ค่านี้เป็นตัวเศษของสมการมวลเปอร์เซ็นต์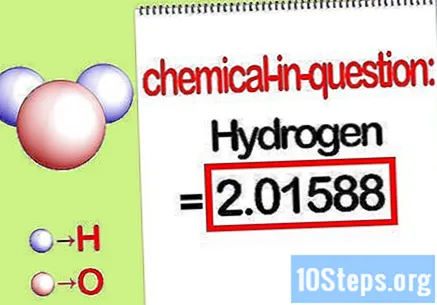
- ตัวอย่างเช่นมวลไฮโดรเจนของสารประกอบคือ 2.01588 g / mol (มวลของอะตอมไฮโดรเจนสองโมล)
- แทนตัวแปรในสูตรมวลเปอร์เซ็นต์ หลังจากกำหนดค่าสำหรับแต่ละตัวแปรแล้วให้แทนที่ค่าเหล่านั้นในสมการที่กำหนดไว้ในขั้นตอนแรก: มวลเปอร์เซ็นต์ = () x 100
- ตัวอย่างเช่นมวลเปอร์เซ็นต์ = () x 100 = () x 100
คำนวณมวลเปอร์เซ็นต์ ตอนนี้สมการถูกสร้างขึ้นแล้วให้แก้เพื่อคำนวณมวลเปอร์เซ็นต์ หารมวลของธาตุด้วยมวลรวมของสารประกอบแล้วคูณด้วย 100 ผลลัพธ์ที่ได้จะเป็นมวลเปอร์เซ็นต์ขององค์ประกอบทางเคมี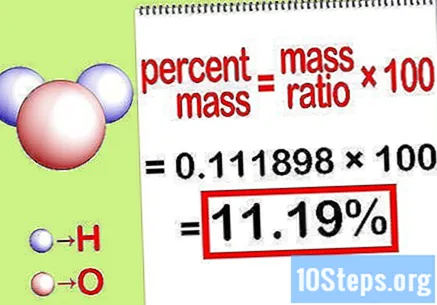
- ตัวอย่างเช่นเปอร์เซ็นต์มวล = () x 100 = 0.111189 x 100 = 11.18% ดังนั้นเปอร์เซ็นต์มวลของอะตอมไฮโดรเจนในโมเลกุลของน้ำจึงเท่ากับ 11.18%