
เนื้อหา
สาขาเคมี อิเล็ก เป็นการวัดแรงดึงดูดที่อะตอมกระทำต่ออิเล็กตรอนในพันธะ อะตอมที่มีค่าอิเล็กโตรเนกาติวิตีสูงจะดึงดูดอิเล็กตรอนที่มีความเข้มสูงในขณะที่อะตอมที่มีค่าอิเล็กโทรเนกาติวิตีต่ำจะทำด้วยความเข้มเพียงเล็กน้อย ค่าเหล่านี้ใช้เพื่อทำนายว่าอะตอมที่แตกต่างกันจะทำงานอย่างไรเมื่อเชื่อมต่อกันทำให้หัวข้อนี้เป็นทักษะที่สำคัญในวิชาเคมีพื้นฐาน
ขั้นตอน
วิธีที่ 1 จาก 3: แนวคิดพื้นฐานของอิเล็กโทรเนกาติวิตี
เข้าใจว่าพันธะเคมีเกิดขึ้นเมื่ออะตอมใช้อิเล็กตรอนร่วมกัน ในการทำความเข้าใจเกี่ยวกับอิเล็กโทรเนกาติวิตีสิ่งสำคัญคือต้องเข้าใจก่อนว่า "ลิงค์" คืออะไร อะตอมสองอะตอมใด ๆ ในโมเลกุลที่ "เชื่อมต่อ" ซึ่งกันและกันในแผนภาพโมเลกุลจะถูกกล่าวว่ามีพันธะระหว่างกัน โดยพื้นฐานแล้วนั่นหมายความว่าพวกมันใช้อิเล็กตรอนร่วมกันสองชุด - แต่ละอะตอมมีส่วนทำให้อะตอมเป็นพันธะ
- เหตุผลที่ชัดเจนเกี่ยวกับสาเหตุที่อะตอมแบ่งอิเล็กตรอนและสร้างพันธะร่วมกันไม่สอดคล้องกับจุดสำคัญของบทความนี้ หากคุณต้องการเรียนรู้เพิ่มเติมให้ค้นหาแนวคิดพื้นฐานของพันธะเคมีในอินเทอร์เน็ต
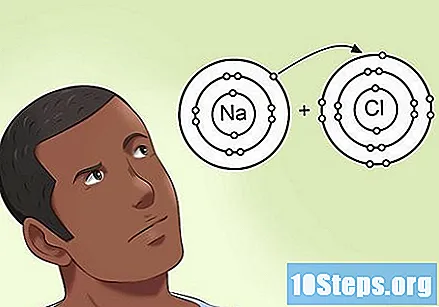
ทำความเข้าใจว่าอิเล็กโทรเนกาติวิตีมีผลต่ออิเล็กตรอนที่อยู่ในพันธะอย่างไร เมื่ออะตอมสองอะตอมใช้อิเล็กตรอนสองตัวร่วมกันในพันธะจะไม่มีการแบ่งปันที่เท่าเทียมกันระหว่างทั้งสอง เมื่อหนึ่งในนั้นมีอิเล็กโตรเนกาติวิตีสูงกว่าอะตอมที่ติดอยู่มันจะทำให้อิเล็กตรอนทั้งสองเข้าใกล้ตัวเองมากขึ้น อะตอมที่มีค่าอิเล็กโทรเนกาติวิตีสูงมากสามารถดึงอิเล็กตรอนไปด้านข้างในพันธะได้เกือบจะยกเลิกการแบ่งปันกับอีกฝ่าย- ตัวอย่างเช่นในโมเลกุล NaCl (โซเดียมคลอไรด์) อะตอมของคลอรีนมีค่าอิเล็กโทรเนกาติวิตีและโซเดียมสูงซึ่งมีค่าอิเล็กโทรเนกาติวิตีต่ำ ในไม่ช้าอิเล็กตรอนจะถูกดึง ต่อคลอรีน และ ห่างจากโซเดียม.

ใช้ตารางอิเล็กโทรเนกาติวิตีเป็นข้อมูลอ้างอิง ตารางอิเล็กโตรเนกาติวิตีแสดงองค์ประกอบที่จัดเรียงเหมือนกับตารางธาตุ แต่แต่ละอะตอมมีสัญลักษณ์อิเล็กโตรเนกาติวิตี สามารถพบได้ในตำราเคมีหลายเล่มในบทความทางเทคนิคและบนอินเทอร์เน็ต- นี่คือตารางอิเล็กโทรเนกาติวิตีที่ยอดเยี่ยม โปรดทราบว่ามันใช้สเกลอิเล็กโทรเนกาติวิตีแบบพอลลิงซึ่งเป็นเรื่องปกติมากขึ้น อย่างไรก็ตามมีวิธีอื่นในการวัดค่าอิเล็กโทรเนกาติวิตีซึ่งหนึ่งในนั้นจะแสดงด้านล่าง
จำแนวโน้มค่าอิเล็กโทรเนกาติวิตีเพื่อประมาณการได้ง่าย หากคุณไม่มีตารางอิเล็กโตรเนกาติวิตีอยู่ในมือคุณยังคงสามารถประมาณค่านี้ตามตำแหน่งของคุณในตารางธาตุได้ ตามกฎทั่วไป:- อิเล็กโทรเนกาติวิตีของอะตอม เพิ่มขึ้น เมื่อคุณย้ายไปที่ไฟล์ ขวา ในตารางธาตุ
- อิเล็กโทรเนกาติวิตีของอะตอม เพิ่มขึ้น ในขณะที่คุณย้ายไป ขึ้น ในตารางธาตุ
- ดังนั้นอะตอมที่อยู่ที่มุมขวาบนจึงมีค่าอิเล็กโทรเนกาติวิตีสูงที่สุดและอะตอมที่อยู่มุมล่างซ้ายจะมีค่าต่ำสุด
- ตัวอย่างเช่นในตัวอย่าง NaCl ก่อนหน้านี้คุณสามารถระบุได้ว่าคลอรีนมีค่าอิเล็กโทรเนกาติวิตีสูงกว่าโซเดียมเนื่องจากเกือบจะอยู่ที่จุดสูงสุดด้านขวา ในทางกลับกันโซเดียมจะอยู่ทางด้านซ้ายของตารางซึ่งทำให้เป็นหนึ่งในอะตอมที่มีค่าน้อยที่สุด
วิธีที่ 2 จาก 3: การค้นหาการเชื่อมต่อด้วยอิเล็กโทรเนกาติวิตี
ค้นหาความแตกต่างของอิเล็กโทรเนกาติวิตีระหว่างอะตอมทั้งสอง เมื่ออะตอมสองอะตอมเชื่อมโยงกันความแตกต่างระหว่างค่าอิเล็กโทรเนกาติวิตีของพวกมันจะเผยให้เห็นคุณภาพของพันธะนั้นมากมาย ลบค่าที่น้อยที่สุดจากค่าที่มากที่สุดเพื่อหาความแตกต่าง
- ตัวอย่างเช่นหากเรากำลังดูโมเลกุล HF เราจะลบค่าอิเล็กโตรเนกาติวิตีของไฮโดรเจน (2.1) ออกจากฟลูออรีน (4.0) 4.0 - 2.1 = 1,9.
ถ้าความแตกต่างต่ำกว่า 0.5 พันธะคือโควาเลนต์และไม่มีขั้ว ที่นี่อิเล็กตรอนจะใช้ร่วมกันในระดับเกือบเท่ากัน พันธะเหล่านี้ไม่ก่อตัวเป็นโมเลกุลที่มีประจุแตกต่างกันมากที่ปลายทั้งสองข้าง พันธะเชิงขั้วมักจะหักยากมาก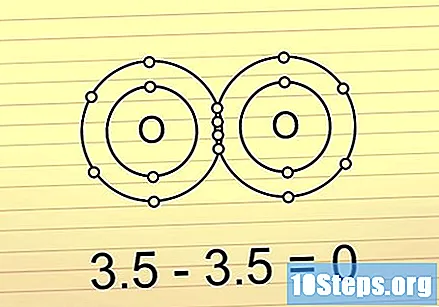
- ตัวอย่างเช่นโมเลกุล O2 นำเสนอการเชื่อมต่อประเภทนี้ เนื่องจากโมเลกุลของออกซิเจนทั้งสองมีค่าอิเล็กโทรเนกาติวิตีเท่ากันความแตกต่างระหว่างโมเลกุลจึงมีค่าเท่ากับ 0
ถ้าความแตกต่างอยู่ระหว่าง 0.5 ถึง 1.6 พันธะคือโคเวเลนต์และมีขั้ว พันธะเหล่านี้มีอิเล็กตรอนที่ปลายด้านหนึ่งมากกว่าอีกด้าน สิ่งนี้ทำให้โมเลกุลเป็นลบมากขึ้นเล็กน้อยในตอนท้ายโดยมีอิเล็กตรอนมากขึ้นและมีค่าบวกเพิ่มขึ้นเล็กน้อยในตอนท้ายโดยไม่มีพวกมัน ความไม่สมดุลของประจุในพันธะเหล่านี้ทำให้โมเลกุลมีส่วนร่วมในปฏิกิริยาเฉพาะบางอย่าง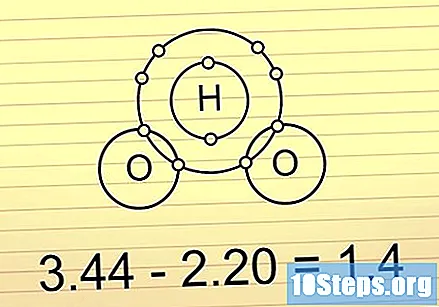
- ตัวอย่างที่ดีคือโมเลกุล H2O (น้ำ) O เป็นอิเล็กโทรเนกาติวิตีมากกว่า H สองตัวดังนั้นมันจึงทำให้อิเล็กตรอนเข้าใกล้และทำให้โมเลกุลทั้งหมดเป็นลบบางส่วนที่ปลาย O และเป็นบวกบางส่วนที่ปลาย H
ถ้าความแตกต่างมากกว่า 2 พันธะจะเป็นไอออนิก ในพันธะเหล่านี้อิเล็กตรอนจะอยู่ที่ปลายด้านหนึ่งอย่างสมบูรณ์ อะตอมอิเล็กโทรเนกาติวิตีส่วนใหญ่จะได้รับประจุลบและอะตอมที่มีอิเล็กโทรเนกาติวิตีน้อยที่สุดจะได้รับประจุบวก พันธะประเภทนี้ช่วยให้อะตอมสามารถทำปฏิกิริยากับอะตอมอื่น ๆ หรือแยกออกจากกันด้วยอะตอมที่มีขั้ว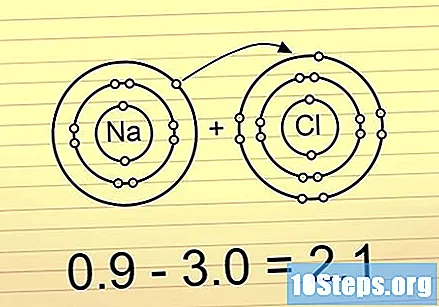
- ตัวอย่างคือ NaCl (โซเดียมคลอไรด์) คลอรีนเป็นอิเล็กโทรเนกาติวิตีมากจนดึงอิเล็กตรอนทั้งสองจากพันธะเข้าหากันทิ้งโซเดียมที่มีประจุบวก
หากความแตกต่างอยู่ระหว่าง 1.6 และ 2 ให้มองหาโลหะ ถ้า ที่นั่น โลหะที่มีอยู่ในพันธะแสดงว่าเป็น อิออน. หากมีอโลหะอื่น ๆ พันธะคือ โควาเลนต์ขั้วโลก.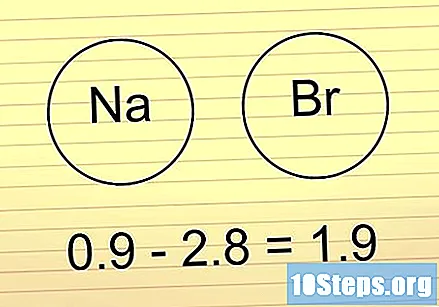
- โลหะประกอบด้วยอะตอมส่วนใหญ่ทางด้านซ้ายและตรงกลางของตารางธาตุ หน้านี้มีตารางแสดงว่าธาตุใดเป็นโลหะ
- ตัวอย่าง HF ก่อนหน้าของเราอยู่ในกลุ่มนั้น เนื่องจาก H และ F ไม่ใช่โลหะพันธะจึงเป็น โควาเลนต์ขั้วโลก.
วิธีที่ 3 จาก 3: ค้นพบ Mulliken Electronegativity
ค้นหาพลังงานไอออไนเซชันแรกของอะตอมของคุณ ค่าอิเล็กโทรเนกาติวิตีของมัลลิเคนประกอบด้วยวิธีการวัดที่แตกต่างจากที่พบในตาราง Pauling ด้านบนเล็กน้อย ในการหาค่าของอะตอมหนึ่ง ๆ ให้ค้นหาพลังงานไอออไนเซชันแรกของคุณ นี่คือพลังงานที่จำเป็นในการทำให้อะตอมปลดปล่อยอิเล็กตรอนตัวเดียว
- ค่านี้อาจพบได้ในวัสดุอ้างอิงทางเคมี หน้านี้มีตารางที่ดีที่คุณสามารถใช้ได้ (เลื่อนลงเพื่อค้นหา)
- ตัวอย่างเช่นสมมติว่าคุณต้องการหาค่าอิเล็กโทรเนกาติวิตีของลิเธียม (Li) คืออะไร ในตารางในหน้าด้านบนเราจะเห็นว่าพลังงานไอออไนเซชันแรกเทียบเท่ากับ 520 กิโลจูล / โมล.
ค้นหาว่าความสัมพันธ์ของอิเล็กตรอนของอะตอมคืออะไร นี่คือการวัดพลังงานที่ได้จากการเพิ่มอิเล็กตรอนเข้าไปในอะตอมเพื่อสร้างไอออนลบ อีกครั้งนี่คือสิ่งที่ควรพบในเอกสารอ้างอิง หน้านี้มีแหล่งข้อมูลที่สามารถเป็นประโยชน์
- ความสัมพันธ์ทางอิเล็กทรอนิกส์ของลิเธียมเท่ากับ 60 กิโลจูลโมล.
แก้สมการอิเล็กโทรเนกาติวิตีของ Mulliken เมื่อใช้ kJ / mol เป็นหน่วยพลังงานสมการอิเล็กโทรเนกาติวิตีของ Mulliken สามารถเขียนเป็น ENMulliken = (1.97 × 10) (จผม + จและ) + 0,19. ใส่ข้อมูลที่ทราบลงในสมการและหาค่าของ ENMulliken.
- ในตัวอย่างของเราเราจะมาถึงความละเอียดต่อไปนี้:
- ENMulliken = (1.97 × 10) (จผม + จและ) + 0,19
- ENMulliken = (1,97 × 10)(520 + 60) + 0,19
- ENMulliken = 1,143 + 0,19 = 1,333
- ในตัวอย่างของเราเราจะมาถึงความละเอียดต่อไปนี้:
เคล็ดลับ
- นอกจากเครื่องชั่ง Pauling และ Mulliken แล้วยังมีเครื่องชั่งอิเล็กโทรเนกาติวิตีอื่น ๆ เช่น Allred-Rochow, Sanderson และ Allen แต่ละตัวมีสมการของตัวเองสำหรับการคำนวณอิเล็กโทรเนกาติวิตี (และบางส่วนอาจซับซ้อนมาก)
- อิเล็ก ไม่มีหน่วยวัด.


